Hogyan lehet megtalálni a protonok, elektronok és neutronok számát?
Szerző:
Roger Morrison
A Teremtés Dátuma:
27 Szeptember 2021
Frissítés Dátuma:
1 Július 2024

Tartalom
- szakaszában
- 1. rész Számítsa ki a protonok, elektronok és neutronok számát
- 2. rész Számolja ki az elektronok számát egy ionban
A neutronok, elektronok és protonok a három fő részecske, amelyek atomot alkotnak. Mint kitalálható, a protonok pozitív töltéssel rendelkeznek, az elektronok negatív töltéssel bírnak, a neutronok pedig csak semleges részecskék. Az elektronok tömege nagyon kicsi. A neutronok és protonok azonban hasonló tömeggel rendelkeznek. Egy atom protonok, elektronok és neutronok számának megállapításához elegendő megvizsgálni az elemek periodikus tábláját, más néven Mendelejev táblázatát.
szakaszában
1. rész Számítsa ki a protonok, elektronok és neutronok számát
-
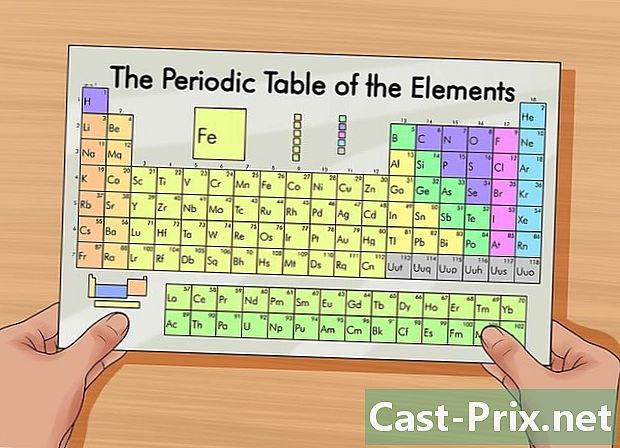
Szerezzen egy időszakos tételeket. Ez a táblázat segít megtalálni a protonok, elektronok és neutronok számát egy elemben. Ez egy táblázat, amely az elemeket atomszerkezetük szerint mutatja be. A színkód megkülönbözteti a különböző elemeket. Minden elemet egy, kettő vagy három betűből álló szimbólum jelöl. A táblázat más információkat is tartalmaz, például az atomtömeg és az egyes elemek atomszámát.- Ez a táblázat megtalálható az interneten történő keresés vagy egy kémiai könyv között.
- A vizsgálatok során rendszerint lehetővé teszi az elemek periodikus táblázatainak használatát.
-
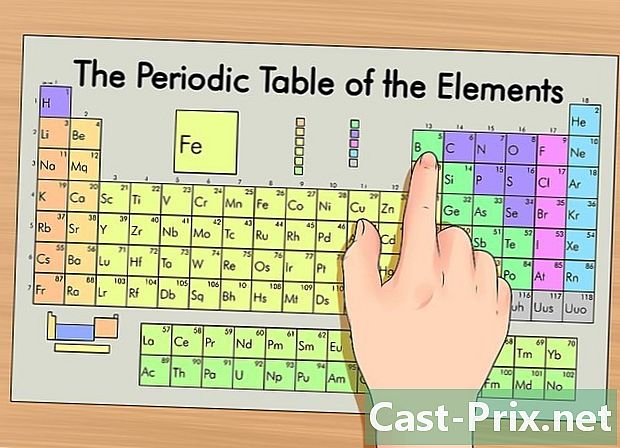
Azonosítsa az elemet a periódusos táblán. A táblázatban az elemeket atomszámuk szerint csoportosítják. Három fő csoportra osztják őket: fémek, nemfémek és metalloidok (félfémek). Egyéb csoportok az alkálifémek, a halogének és a nemesgázok.- Könnyebb megtalálni az elemet a tömbben annak csoportja (oszlop) vagy periódusa (sor) segítségével.
- Ha nem ismeri az elem tulajdonságait, akkor keresse meg annak szimbólumát.
-
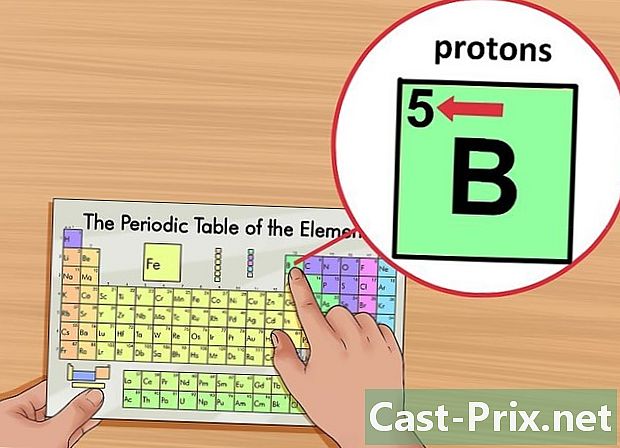
Keresse meg az elem atomszámát. Ezt a számot a mező bal felső sarkában, az elem szimbólum fölött jelölik. Az atomi szám megadja a szóban forgó elemet alkotó protonok számát.- Például a (B) bór atomszáma 5. Tehát 5 protonnal rendelkezik.
-

Határozzuk meg az elektronok számát. Egy atommag magában foglalja a protonokat, amelyek pozitív töltésű részecskék. Az elektronok negatív töltésű részecskék. Ezért a semleges elem protonjai és elektronjai azonosak lesznek.- Például a (B) bór atomszáma 5, tehát 5 protonja és 5 elektronja van.
- Ha ez pozitív vagy negatív ion, akkor a protonok száma és az elektronok száma különbözik. Ki kell számítania őket. Az oroszlán töltését kis méretű betűk jelzik egy exponenssel a megfelelő elem után.
-

Keresse meg az elem atomtömegét. Ez a lépés lehetővé teszi a neutronok számának meghatározását. Először meg kell határoznia az elem atomtömegét vagy atomtömegét. Ez a nullapont képviseli az elem atomjainak átlagos tömegét. Az elem szimbóluma alatt van feltüntetve.- Feltétlenül kerekítse az elem atomtömegét a legközelebbi egész számra. Így a bór atomtömege 10,811, de 11-re kell gördülnie.
-

Végezzük a különbséget az atomszám és az atomtömeg között. A neutronok számának kiszámításához különbséget kell tennie az atomszám és az atomtömeg között. Ne felejtsük el, hogy már ismeri az atomszámot. Egyszerűen megegyezik a protonokéval.- Bór esetén: 11 (atomtömeg) - 5 (atomszám) = 6 neutron
2. rész Számolja ki az elektronok számát egy ionban
-

Keresse meg egy ion elektromos töltését. Ez a szám exponensen jelenik meg az elem szimbólum után. Az ion olyan atom, amelynek pozitív vagy negatív töltése van az elektronok hozzáadása vagy elnyomása miatt. Az atom protonjai nem változnak. Egy ionban azonban az elektronok száma megváltozik.- Mivel egy elektron negatív töltésű, egy vagy több elektron eltávolítása után pozitívvá válik. Másrészt az elektronok hozzáadása azzal a hatással jár, hogy a töltés negatívvá válik.
- Például az N terhelése -3. Másrészről Ca értéke +2.
- Ne felejtse el, hogy erre a számításra nincs szükség, ha az elem szimbólumát nem követi exponens.
-

Távolítsa el a töltést az atomszámból. Eredetileg egy pozitív töltésű ion olyan atom, amely elvesztette elektronjait. Az elektronok számának megállapításához ki kell vonni a kiegészítő töltéseket az atomszámból. Ha az oroszlán pozitív, akkor a protonok száma nagyobb, mint az elektronoké.- Például a Ca töltése +2. Ennek eredményeként 2 elektron veszített el az eredeti állapotához képest. A kalcium atomszáma 20, tehát az oroszlánnak 18 elektronja van.
-

Adjunk egy töltést a negatív ionok atomszámához. Ha egy ion negatív töltésű, a latom extra elektronokkal rendelkezik. Az elektronok teljes számának kiszámításához elegendő a kiegészítő töltések számát hozzáadni az atomszámhoz. Ha az oroszlán negatív, kevesebb protonnal rendelkezik, mint az elektron.- Például az N terhelése -3. Tehát még három elektronot hordoz a kezdeti állapotához képest. A lazoták atomszáma 7. Ezért ennek az ionnak 10 elektronja van.